Indikator asam-basa merupakan salah satu elemen kunci dalam dunia kimia yang membantu menentukan tingkat keasaman atau kebasaan suatu larutan. Penggunaan indikator ini sangat penting dalam berbagai bidang, mulai dari laboratorium kimia hingga industri.
Lalu apa itu indikator asam-basa? dan apa fungsi dari indikator ini di bidang kimia dan industri? Penjelasan lengkap dari pertanyaan ini telah kami rangkum pada artikel ini! Mari simak bersama-sama.
Daftar Isi
Pengertian Indikator Asam-Basa
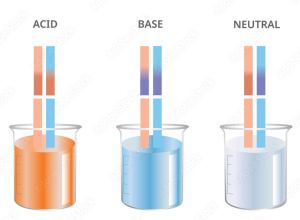
Indikator asam-basa adalah zat kimia yang dapat digunakan untuk menentukan keasaman atau kebasaan suatu larutan. Indikator ini bekerja dengan mengalami perubahan warna pada pH tertentu. pH merupakan suatu ukuran yang menunjukkan tingkat keasaman atau kebasaan suatu larutan, dengan skala pH berkisar antara 0 hingga 14.
Nilai pH 7 dianggap netral, sementara nilai di bawah 7 menunjukkan sifat asam, dan nilai di atas 7 menunjukkan sifat basa atau alkali. Indikator ini memainkan peran penting dalam menentukan sifat larutan untuk berbagai aplikasi, dari pengujian kualitas air hingga pembuatan produk kimia.
Fungsi Indikator Asam-Basa
Indikator asam-basa memiliki peran penting di laboratorium untuk menentukan pH suatu larutan atau menilai keasaman dan kebasaan suatu zat kimia. Beberapa fungsi utama indikator ini yaitu:
- Titik Akhir Titrasi: Indikator asam-basa sering digunakan dalam proses titrasi, di mana larutan titran ditambahkan ke larutan yang dititrasi hingga mencapai titik akhir. Perubahan warna indikator pada titik akhir menandakan selesainya reaksi kimia, dan ini membantu menentukan konsentrasi atau jumlah zat dalam larutan.
- Pengukuran pH: Indikator asam-basa dapat digunakan untuk mengukur pH larutan secara kualitatif. Misalnya kertas lakmus dapat digunakan untuk menunjukkan apakah larutan bersifat asam, basa, atau netral. Indikator lainnya, seperti fenolftalein, bromotimol biru, dan lainnya, memberikan informasi lebih detail tentang kisaran pH larutan.
- Kontrol Kualitas: Dalam laboratorium, indikator asam-basa dapat digunakan untuk mengontrol kualitas suatu produk atau larutan. Misalnya, dalam industri farmasi, indikator dapat digunakan untuk memastikan bahwa larutan obat atau bahan kimia lain memiliki pH yang sesuai dengan spesifikasi tertentu.
- Pemisahan Zat Kimia: Beberapa reaksi kimia memerlukan pengaturan pH tertentu. Indikator asam-basa dapat digunakan untuk mengawasi dan mengontrol pH selama proses reaksi atau pemisahan zat kimia.
- Identifikasi Senyawa: Perubahan warna yang dihasilkan oleh indikator asam-basa dapat digunakan sebagai alat identifikasi senyawa atau kelompok senyawa tertentu dalam campuran kompleks.
- Penelitian Ilmiah: Dalam eksperimen ilmiah, indikator asam-basa dapat digunakan untuk memahami dan menyelidiki sifat-sifat asam-basa suatu zat. Perubahan warna indikator dapat memberikan informasi tentang karakteristik kimia larutan yang diuji.
Syarat Suatu Zat Dapat Digunakan Sebagai Indikator Asam-Basa
Tidak semua zat dapat berfungsi sebagai indikator asam-basa. Beberapa syarat harus terpenuhi agar suatu zat dapat dianggap sebagai indikator yang efektif. Pertama, indikator harus memiliki rentang perubahan warna yang sesuai dengan rentang pH yang ingin diukur. Kedua, indikator harus peka terhadap perubahan pH, sehingga perubahan warna dapat terjadi dengan jelas.
Selain itu, stabilitas zat indikator juga perlu dipertimbangkan agar tidak terjadi perubahan warna yang tidak diinginkan selama penyimpanan atau penggunaan.
Contoh Indikator Asam-Basa
Indikator asam-basa sering digunakan untuk menentukan titik akhir titrasi pada suatu pengujian. Terdapat beberapa indikator asam-basa yang umum digunakan, antara lain:
- Fenolftalein: Fenolftalein adalah indikator yang umum digunakan dalam titrasi asam-basa. Dalam suasana asam, fenolftalein tidak berwarna, tetapi ketika larutan menjadi basa, ia berubah menjadi merah muda cerah.
- Metil Orange: Metil Orange adalah indikator asam-basa yang sering digunakan dalam percobaan dan titrasi. Pada suasana asam, metil orange berwarna jingga cerah, sedangkan pada suasana basa, ia mengubah warnanya menjadi kuning cerah.
- Metil Red: Metil Red adalah indikator asam-basa yang berwarna merah pada suasana asam dan kuning pada suasana basa. Perubahan warna ini terjadi pada rentang pH yang sedikit lebih tinggi dibandingkan dengan metil orange.
- Bromotimol Biru: Bromotimol Biru adalah indikator yang berguna dalam menentukan keasaman atau kebasaan suatu larutan. Pada suasana asam, bromotimol biru berwarna kuning, pada netral berwarna hijau, dan pada suasana basa berubah menjadi biru.
- Litmus: Litmus adalah indikator asam-basa alami yang mudah digunakan. Dalam suasana asam, litmus berwarna merah, sementara dalam suasana basa berwarna biru.
- Bromocesol Green: Bromocesol Green adalah indikator dengan perubahan warna dari kuning (pH asam) menjadi biru (pH basa).
- Alizarin Red S: Alizarin Red S adalah indikator yang berubah warna dari merah pada suasana asam menjadi ungu pada suasana basa.
- Cresol Red: Cresol Red adalah indikator asam-basa yang berwarna merah pada suasana asam dan kuning pada suasana basa.
Setiap indikator memiliki rentang pH yang optimal untuk perubahan warna, sehingga pemilihan indikator harus sesuai dengan kondisi pH yang akan diuji.
Cara Menentukan Indikator Asam-Basa
Menentukan indikator asam-basa dapat dilakukan dengan metode sederhana. Salah satu cara yang umum digunakan adalah dengan mengamati perubahan warna indikator saat ditambahkan ke dalam larutan yang akan diuji.
Selain itu, kertas lakmus juga sering digunakan dengan cara direndam dalam larutan untuk mengukur pH. Metode elektrokimia dan spektrofotometri juga digunakan untuk penentuan pH yang lebih akurat dalam situasi laboratorium yang lebih canggih.
Prinsip Kerja Indikator Asam-Basa
Prinsip kerja indikator asam-basa terkait erat dengan perubahan struktur molekul indikator yang dipengaruhi oleh perubahan konsentrasi ion hidrogen (H+) dalam larutan. Berikut adalah prinsip kerja umum indikator asam-basa:
- Struktur Molekuler Indikator: Indikator asam-basa memiliki struktur molekuler yang dapat mengalami perubahan warna saat terjadi perubahan pH. Struktur ini seringkali melibatkan gugus kimiawi yang berinteraksi dengan ion hidrogen (H+) atau hidroksida (OH-) dalam larutan.
- Perubahan Struktur Molekuler: Pada dasarnya, perubahan struktur molekuler indikator terjadi sebagai respon terhadap perubahan konsentrasi ion hidrogen dalam larutan. Ketika larutan menjadi lebih asam atau lebih basa, gugus-gugus kimiawi dalam molekul indikator mengalami perubahan konformasi atau ikatan kimia yang mengakibatkan perubahan warna.
- Perubahan Warna Terkait dengan pH: Indikator asam-basa biasanya memiliki rentang pH tertentu di mana perubahan warna terjadi. Rentang ini disebut juga sebagai titik perubahan atau titik akhir titrasi. Pada titik ini, keseimbangan antara bentuk asam dan basa dari indikator mencapai titik kritis yang menyebabkan perubahan warna yang teramati.
- Ionisasi dan Disosiasi: Sebagian besar indikator asam-basa merupakan senyawa organik lemah yang dapat mengalami ionisasi atau disosiasi dalam larutan. Misalnya, beberapa indikator mengandung gugus asam karboksilat yang dapat melepaskan atau menerima ion hidrogen tergantung pada pH larutan.
- Equilibrium Reaksi Kimia: Perubahan warna yang diamati pada indikator asam-basa terkait erat dengan mencapai suatu keseimbangan (equilibrium) antara bentuk asam dan bentuk basa dari indikator tersebut. Pada titik keseimbangan ini, jumlah molekul yang berada dalam bentuk asam dan basa adalah sama, dan ini mempengaruhi warna keseluruhan larutan.
Contoh sederhana prinsip kerja ini dapat diilustrasikan dengan fenolftalein. Fenolftalein berwarna tidak berwarna dalam suasana asam, tetapi berubah menjadi merah muda pada suasana basa. Ini terjadi karena fenolftalein mengalami ionisasi atau disosiasi pada titik kritis pH tertentu, menciptakan perubahan warna yang dapat diamati.
Kesimpulan
indikator asam-basa adalah zat kimia yang digunakan untuk menentukan keasaman atau kebasaan suatu larutan dengan mengalami perubahan warna pada pH tertentu. pH adalah ukuran keasaman atau kebasaan larutan, dengan skala antara 0 hingga 14. Indikator ini memiliki berbagai fungsi di laboratorium, termasuk titrasi, pengukuran pH, kontrol kualitas, pemisahan zat kimia, identifikasi senyawa, dan penelitian ilmiah.
Beberapa syarat untuk zat dapat dianggap sebagai indikator efektif melibatkan rentang perubahan warna yang sesuai dengan pH yang diukur, sensitivitas terhadap perubahan pH, dan stabilitas selama penyimpanan atau penggunaan.
Metode penentuan indikator melibatkan pengamatan perubahan warna, penggunaan kertas lakmus, metode elektrokimia, dan spektrofotometri. Prinsip kerja indikator asam-basa berkaitan dengan perubahan struktur molekuler indikator yang dipengaruhi oleh perubahan konsentrasi ion hidrogen dalam larutan, mencapai suatu keseimbangan yang mempengaruhi warna larutan pada titik perubahan pH tertentu.


